|
16.1 |
TRANSMUTATIONS ET RADIOACTIVITÉ ARTIFICIELLE
|
Aux noyaux naturels instables est-il possible d’ajouter, de synthétiser des noyaux artificiels ? Si oui, d'autres questions demandent des réponses
Questions : Objectif : |
1. Découverte de la transmutation artificielle
L’observation des trajectoires bien définies des particules a dans l’air conduisit à une exploration systématique des trajectoires des particules a dans les autres gaz. Dans l’azote, Lord RUTHERFORD (1919) trouva que la plupart des rayons s’arrêtent au bout d’un parcours de 7 cm, mais que certaines particules plus rares étaient encore capables de produire des scintillations à 40 cm. Il put montrer que ces particules étaient des protons rapides produits pas le bombardement des atomes d’azote par les rayons a. Mais l’énergie cinétique des protons est beaucoup plus grande que l’énergie cinétique des particules a. On ne pouvait donc admettre l’existence d’une simple collision.
Il fallait donc supposer que la particule a et le noyau d’azote forment un "complexe" contenant, sous forme d’énergie interne la plus grande part de l’énergie cinétique de la particule a. La chambre de WILSON (voir Chapitre 15).permit de voir ce qu’il advenait du complexe formé. Deux traces sont observées après collision de la particule a et du noyau d’azote. L’une est celle du proton, l’autre est celle d’une particule très fortement ionisante donc lourde et de faible vitesse. Un simple calcul arithmétique montre que l’on a formation d’un noyau d’oxygène après départ du proton: il y a transmutation artificielle (induite par le rayonnement a) de l’atome d’azote-14 en oxygène-17.
|
16.1 |
La source de rayons a est du
![]()
qui émet un rayonnement de 7,68 MeV. Le noyau complexe
![]()
est écrit pour des raisons de clarté mais il est très instable et explose instantanément. Cette réaction est le type d’une réaction nucléaire. Elle peut s’écrire en notation abrégée.
|
16.2 |
La possibilité d’éjection d’un proton à partir du noyau de l’atome confirmait le fait que cette particule pouvait être un des blocs constituant du noyau.
2. Le neutron
La découverte de RUTHERFORD amena la recherche systématique d’autres types de transmutation. Les recherches s’orientèrent vers les noyaux légers puisque ceux-ci avaient moins de chance de repousser les particules a. C’est ainsi que W. BOTHE et H. BECKER (1930) découvrirent un rayonnement extrêmement pénétrant provenant du béryllium
![]()
bombardé par les particules a. Après avoir pensé à des photons du type g, J. CHADWICK (1932) montra que ce rayonnement devait être composé de particules neutres de masse analogue à celle du proton.
La réaction nucléaire pouvait s’écrire :
|
16.3 ou bien : |
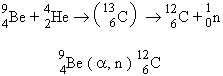 |
Ici, encore, le noyau de carbone-13, formé dans la réaction 16.3, est très instable (car très énergétique) et se désintègre instantanément libérant un noyau de carbone-12 et un neutron..
Les neutrons ne sont pas ionisants et ne peuvent être
observés à la chambre de WILSON. Par contre ils peuvent éjecter les protons des
molécules telles que CH4. Ces protons sont alors observés directement par
leur trace. Les neutrons ayant un libre parcours moyen très élevé, en particulier dans
des enceintes vides, on peut aisément déterminer leur vitesse en utilisant un sélecteur
de vitesse (deux disques éloignés d’une distance ![]() ayant chacune une fente
convenablement placée et tournant à la même vitesse). Cette mesure permet d’obtenir des
informations précieuses quant à l’énergie libérée par la réaction nucléaire.
ayant chacune une fente
convenablement placée et tournant à la même vitesse). Cette mesure permet d’obtenir des
informations précieuses quant à l’énergie libérée par la réaction nucléaire.
L’éjection de neutrons par le noyau suggère l’hypothèse que le neutron est également un bloc constituant. On pourrait évidemment en dire autant de la particule a. On admet actuellement que les constituants élémentaires du noyau sont bien les protons et les neutrons, mais que la particule a constitue une association très stable de deux protons et de deux neutrons avec une énergie de liaison relativement grande.
La diffusion
Lorsqu’une particule animée d’une grande vitesse entre en collision avec une particule au repos, elle rebondit parfois purement et simplement. C’est le phénomène de diffusion élastique auquel s’appliquent les lois classiques de conservation des quantités de mouvement et de l’énergie. On montre que l’énergie de recul de la particule cible est d’autant plus importante que les éléments "projectile" et "cible" ont une masse voisine, sinon égale.
Soient deux particules, l’une de masse m1 animée d’une vitesse u1, et l’autre de masse m2 au repos. Supposons que la collision se fasse selon la ligne des centres. En appliquant les principes de conservation de l’énergie et de la quantité de masse on peut écrire :
m1 u1 = m1 u1' + m2 u2'
et
![]()
Ces deux équations permettent de calculer les vitesses u1' et u2' des deux particules après collision :
|
16.4 |
|
L’énergie cinétique gagnée par la deuxième particule (celle qui était au repos) est égale à l’énergie perdue par la particule incidente : DE1 = E2'. On peut montrer que la fraction d’énergie perdue par la particule de masse m1 est telle que :
|
16.5 |
|
On peut montrer que ce dernier rapport est maximum lorsque les deux particules ont la même masse. Plus précisément, si m1 = m2, DE1/E1 = 1. Il y a alors transfert intégral d’énergie cinétique. Si au contraire les deux particules sont de masse très différentes, par exemple si m1 << m2, DE1/E1 @ 4 m1/m2, l’énergie transmise est négligeable. Ce calcul constitue un cas limite. En effet, les collisions se font rarement selon la ligne des centres. D’autre part, si l’eau est le modérateur, les atomes d’hydrogène, afin d’effectuer le recul impliqué par le transfert d’énergie cinétique, doivent aussi rompre le lien chimique qui les relie à la molécule d’eau.
Ainsi, pour "refroidir" des neutrons (les freiner), les atomes d’hydrogène devraient être d’excellents modérateurs. Ils ont cependant un défaut majeur: ils captent les neutrons dans une réaction nucléaire de type H(n, g)D. Tout autre élément léger est acceptable pourvu qu’il n’y ait pas de réactions nucléaires parallèles. D’où l’usage de l’eau lourde (cas du réacteur CANDU), du graphite, ... comme modérateur.
La réaction de capture neutronique - la section efficace.
Lorsque l’on étudie l’efficacité de la capture neutronique par un noyau quelconque pour amorcer une réaction nucléaire, on remarque que l’énergie cinétique des neutrons projectiles a une influence considérable sur cette efficacité. On remarque, en général, qu’elle est d’autant plus faible que l’énergie cinétique (la vitesse) des neutrons est grande. Ce n’est qu’une tendance qu’il faut cependant vérifier cas par cas. Pour différentes raisons qu’il est difficile d’expliquer ici, on mesure cette efficacité de capture en barns : c’est une surface -1 barn = 10-28 m2. Cette surface pourrait être celle du cercle centré sur le noyau cible, à l’intérieur du quel cercle, les neutrons y passant seraient captés par le noyau cible.
3. La radioactivité artificielle
Irène CURIE et Frédéric JOLIOT découvrirent en 1934 que plusieurs éléments légers, après avoir été bombardés par des particules a restent radioactifs après le bombardement : c’est la radioactivité artificielle ou provoquée. Par exemple, l’aluminium subit la réaction nucléaire suivante :
| suivie de |
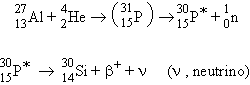 |
La déflexion magnétique des particules émises montre que ce sont des électrons positifs, particules déjà découvertes à la suite de l’étude des rayons cosmiques. Cette radioactivité a une période de 2,5 minutes et si on sépare chimiquement le phosphore et l’aluminium, on constate que toute l’activité est concentrée dans le phosphore. C’est donc
![]()
qui est l’élément radioactif, transformé en un élément stable
![]()
La découverte et l’utilisation des neutrons rendit plus facile l’étude des réactions nucléaires. En effet, les neutrons ne sont pas repoussés par les noyaux et la probabilité de collision est donc augmentée. Un grand nombre d’éléments radioactifs, couvrant toute la classification périodique ont été découverts par bombardement de neutrons. Il est inutile de donner une longue liste de toutes ces réactions qui peut être trouvée dans les livres spécialisés.
Voici quelques réactions particulièrement intéressantes. La réaction peut être "neutron-alpha" (on indique également la période de l’élément ainsi synthétisé) :
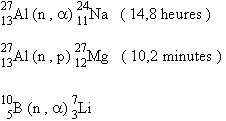 |
|
| ou "neutron-proton" | |
| La réaction ne conduit pas toujours à un produit radioactif, par exemple : |
|
est stable. |
Cette réaction, ayant une grande probabilité est utilisée pour mesurer l’intensité d’un faisceau de neutrons. Une chambre d’ionisation contenant du bore répond aux neutrons par l’émission a qui produit l’ionisation. Le bore est un poison des réacteurs atomiques pour la même raison (facilité d’absorption des neutrons).
La réaction la plus importante est la capture de neutron. Un isotope de masse plus élevée est produit. Il peut être stable ou instable. Cette réaction qui est plus probable avec des neutrons lents se produit également avec l’aluminium. Après capture du neutron, son énergie de liaison devient disponible et fournit donc l’énergie nécessaire à l’émission d’un photon g :
![]()
|
|
est radioactif. |
Il se transforme en
|
|
après émission d’un électron. |
Tout se passe comme si le neutron en excès devenait proton avec émission d’un électron. On a donc finalement transformé un élément en élément de numéro atomique immédiatement supérieur. La capture de neutron et plus probable avec des neutrons lents. On produit ces neutrons lents ou neutrons thermiques (car leur énergie cinétique est voisine de kT) en les ralentissant par collision contre des protons (eau) ou des atomes de carbone (graphite).
|
|
Figure 16.1. Coordonnées de réactions nucléaires.
On remarque que les énergies mises en jeu sont de l'ordre du
million d'électronvolts.
Les
radioéléments et la médecine
La
synthèse de radioéléments est mise à profit par le génie médical. En
effet, pour certains examens médicaux, l’usage de radioéléments permet
d’obtenir des clichés très révélateurs de lésions ou de pathologies
permettant ainsi l’administration de traitements appropriés.
Le choix de ces radioéléments est soumis à plusieurs contraintes. Citons :
1-
la non toxicité du radioélément ou de la combinaison moléculaire qui
le porte;
2-
sa relative facilitée d’élimination (transformation hépatique éventuelle)
par les voies naturelles;
3-
sa demi-vie qui doit se situer approximativement entre une heure et une
semaine;
4-
sa performance exprimées en termes d’imagerie (performance technique);
5-
l’aisance de sa manipulation; et sans doute,
6-
son coût d’utilisation.
On
devrait aussi parler de performance médicale permettant d’associer clairement
une pathologie à un cliché scintigraphique. Cette
performance dépend souvent davantage de la combinaison moléculaire qui
comprend le radioélément. On
dispose ainsi d’une quinzaine de candidats (Tableau 16.1).
| Radioélément | Rayonnement | Période |
| Fluor 18 | b+ | 108 min |
| Technétium 99m | g | 6,02 h |
| Iode 123 | g | 13,3 h |
| Yttrium 90 | b- | 64,1h |
| Indium 111 | g | 67,3 h |
| Rhénium 186 | g , b- | 3,77 j |
| Iode 124 | g , b+ | 4,18 j |
| Iode 131 | g , b- | 8,02 j |
| Extrait de J. P. Meunier, G. Schorsch et R. Zimmermann, L’Actualité chimique, 49-56, nov.-déc. 2003. | ||
Le technétium-99 métastable lui-même, issu de la transmutation spontanée du molybdène-99, est probablement le plus couramment utilisé dans des examens scintigraphiques de l’appareil squelettique, du foie, des poumons et des reins
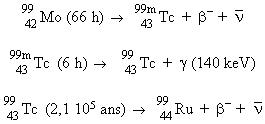
La majorité des émissions en radioactivité proviennent du
noyau : a,
b-,
b+ et rayonnement
g. Quant aux rayons X ils
proviennent plutôt du nuage électronique, donc de l'atome. L'émission du
rayonnement a est une caractéristique
des noyaux lourds. Beaucoup
d’éléments artificiels sont fabriqués par capture d’un proton ou d’un neutron
par un noyau stable « père ». Il
s’ensuit un déséquilibre au sein du noyau « fils » qui cherche à retrouver une
stabilité. On peut envisager deux
cas :
1-
un excès de neutrons : l’un de ceux-ci va se transformer
dans le noyau fils pour donner un
proton qui demeure au sein du noyau et un électron qui éjecté en même temps
qu’un neutrino. C’est le cas de la
réaction suivante :
31P
(n,
g)
32P (b,
neutrino) 32S
2-
un défaut de neutrons : un proton capte alors un
électron du nuage électronique pour se transformer en neutron.
La lacune créée au sein du nuage électronique conduit à l’apparition d’un
rayonnement X.
Dans tous ces cas il y a un rayonnement
g associé.
Il va de soi que toutes ces réactions obéissent à des règles élémentaires de conservation d’énergie, de matière, de matière-énergie et de quantité de mouvement. Par exemple, ces réactions doivent respecter la conservation du nombre de nucléons :
a- Bilan de matière
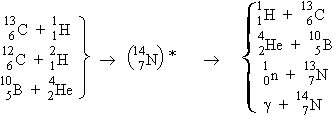
b- Bilan d’énergie
De la même manière, l’énergie disponible conditionne la faisabilité des réactions. Ainsi, pour passer les barrières de potentiel, l’énergie cinétique des particules doit être suffisante. Ainsi le bombardement de l’aluminium-27 par un rayonnement a produit des noyaux de phosphore-31 excités. Au lieu de redescendre vers l’état stable du phosphore, ils émettent un proton et forment des noyaux de silicium diversement excités (Fig. 16.2A). Le nombre de protons ainsi produits peut être mesuré en fonction de l’énergie qu’ils transportent. La figure 16.2B traduit les observations.
|
|
Figures 16.2. Bilans dans la réaction nucléaire : |
5. Accélération des particules
La radioactivité naturelle produit des particules a avec une énergie maximum de l’ordre de 10 MeV. Les neutrons, plus pénétrants, sont cependant produits avec des énergies du même ordre de grandeur. Il était évidemment intéressant d’obtenir des particules plus énergétiques pour provoquer d’autres réactions nucléaires. Nous renvoyons aux livres d’introduction à la Physique Atomique pour le principe et la description de ces machines. En 1932, en utilisant un accélérateur de protons de 500 keV, on observa l’émission de rayonnement a à partir de la réaction suivante :
|
16.6 |
C’est à l’aide de tels appareils que certains éléments transuraniens ont pu être synthétisés. Ce fut le cas de l’élément 106 qui a été préparé par deux laboratoires différents :
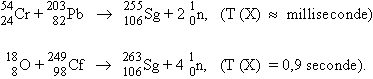
Tableau 16.2. Quelques éléments transuraniens et et leur temps de demi-vie
|
Éléments |
Nom | Symbole* | Exemples de réactions de synthèse des noyaux** |
Temps(1/2 vie) /s |
| 104 | Rutherfordium | Rf |
 |
75 |
| 105 | Dubnium | Db | 34 | |
| 106 | Seaborgium | Sg | 25 | |
| 107 | Bohrium | Bh | 10 | |
| 108 | Hassium | Hs | 5 | |
| 109 | Meitnerium | Mt | 0,2 | |
| 110 | Darmstadtiuma | Ds | 0,000 163 | |
| 111 | Roentgeniuma | Rg | 0,0015 | |
| 112 | Coperniciuma | Cn | 0,0007c | |
| 114 | Fleroviumb | Fl | 2,6 | |
| 116 | Livermoriumb | Lv | 0,061 | |
| * :
Nomenclature fixée par l'IUPAC (International Union of Pure and Applied
Chemistry); voir C&EN, 12, 24 février 1997, 10, 17 mars
et 8 septembre 1997; ** : Hoffman, D. C. et D. M. Lee, J. Chem. Educ., 76(3), 332-347 (1999) au moins la première moitié du tableau ; a : Approbation par l'IUPAC le 4 novembre 2011; b : le 31 mai 2012; c : L'isotope 285 de cet élément aurait un temps de demi-vie de 29 s. Plusieurs autres éléments jusqu’au numéro atomique 118 sont sur la table de travail des chercheurs. |
||||
D'autres isotopes des éléments apparaissant ci-dessus ont aussi été observés. En général, plus l'élément contient de neutron et plus son temps de demi-vie est long. Ainsi le 270-bohrium a un temps de demi-vie de 69 s et celui du 281 -roentgenium- est de 26 s.
Note : Théoriquement, des chercheurs ont montré qu’il doit exister un îlot de relative stabilité grossièrement centré autour de noyaux constitués de quelque 184 neutrons et de 114 protons. Les noyaux situés au centre de cet îlot devraient avoir des temps de vie relativement longs. En 1999, des laboratoires américains et russes ont annoncé indépendamment l’un de l’autre avoir synthétisé quelques noyaux ayant 114 protons et 173-175 neutrons. Les temps de vie mesurés sont de l’ordre de la milliseconde et plus. La technique de synthèse de ces noyaux repose sur le bombardement de 142Pu par des noyaux de 48Ca (voir Chem. & Engineer. News, 11, 19 juillet 1999, ainsi que la revue de l’ordre des chimistes du Québec : "Chimiste", J.-Cl. Roy, XVI, 8-10 (juin 2001)).
Le 30 novembre 2016, l’IUPAC a annoncé avoir accepté les noms des éléments 113, 115, 117 et 118, respectivement le nihonium, le moscovium, le tennessine et l’organesson : 113Nh, 115Mc, 117Ts et 118Og. Si le mocovium et le tennessine font référence à Moscou et au Tennessee, deux régions particulièrement actives dans la synthèse de ces nouveaux éléments, le mot nihon est une appellation alternative du Japon. Quant à l’organesson, ce mot veut rendre hommage à un chercheur russe (Voir : Chem. & Engineer. News, 5 décembre 2016, page 7).
Nous avons vu que la capture de neutron formait un élément en l’élément de numéro atomique immédiatement supérieur. FERMI et ses collaborateurs tentèrent d’appliquer cette méthode à l’uranium, dernier élément de classification périodique, en espérant pouvoir produire des éléments de numéro atomique plus élevé. Ils furent capables effectivement de mettre en évidence une série de produits inconnus et de réactions nouvelles que l’on peut résumer ainsi :
|
(période de 23 minutes) (période de 2,3 jours) (période 24 100 ans)
|
On pourrait donc considérer le plutonium comme le père du très rare isotope
![]() .
.
On a effectivement, récemment, trouvé des traces de plutonium dans le minerai d’uranium. Il ne peut exister à l’état naturel qu’à l’état de traces, sa période étant courte comparée à la durée des ères géologiques.
En 1938, il semblait bien établi que seules des particules ne dépassant par la masse des particules a pouvaient être éjectées du noyau. Avec l’aide de Lise MEITNER qui fit les calculs appropriés et de Fritz STRASSMANN qui réalisa des analyses chimiques extrêmement minutieuses, Otto HAHN, en fin 1938, montra que dans le bombardement de l’uranium par des neutrons apparaissait également l’élément
![]() .
.
Il fallait donc admettre une véritable cassure du noyau, une fission. L’étude du phénomène à la chambre d’ionisation et à la chambre de WILSON montra l’énorme quantité d’énergie transférée aux produits de la fission.
D’autre part, le processus élémentaire initié par un neutron en produit plusieurs. On peut donc espérer que la réaction s’entretiendra d’elle-même. Plus tard, on trouva que, par suite des réactions secondaires, chaque fission atomique produisait environ 2,5 neutrons. En effet, l’élément fissible est seulement l’uranium-235. L’uranium-238 capte les neutrons comme décrit précédemment. Le plutonium-239 produit à partir de l’uranium-238 est aussi une matière fissible. C’est un produit très intéressant par rapport à 235U car on peut l’isoler par séparation chimique plus facile que la séparation isotopique.
Dans le cas de la fission de l’uranium-235 bombardé par les neutrons lents ou rapides, il y a formation d’une série de divers éléments comme par exemple :
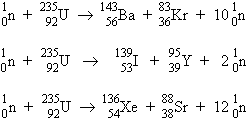
Les produits de fission sont variés. On a cependant constaté que la distribution de ces produits est telle que (Fig. 16.3) :
72 < M < 162.
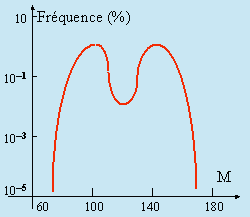 |
Figure 16.3. Fréquence de fission de 235U.
On voit ici la production significative de neutrons, susceptibles de propager la réaction en chaîne. Il faut cependant noter que ces neutrons émis par la fission des noyaux d’uranium ont une énergie cinétique relativement importante : Fig. 16.4. Pour augmenter l’efficacité de la capture neutronique par d’autres noyaux d’uranium, il est nécessaire de ralentir ces neutrons (Fig. 16.5). D’où l’usage de modérateurs. Cet usage permet de diminuer la taille des réacteurs nucléaires puisque "refroidit" le neutron est plus facilement intercepté, récupéré pour l’entretien de la chaîne. Il faut ensuite éviter que l’uranium-235 ne contienne trop d’uranium-238, lequel vient intercepter les neutrons en formant le neptunium et le plutonium. Ces neutrons sont donc perdus par la chaîne. Ce caractère d’explosion en chaîne est évidemment mis à profit dans la bombe nucléaire (bombe A). L’uranium-235 doit être amené au-dessus de la masse critique. Ce phénomène est aussi facilement réalisable avec le plutonium-239.
|
|
Figure16.4. Distribution des énergies cinétiques des neutrons émis par 235U.
|
|
Figure16.5. Section efficace de fission de 235U par des neutrons en fonction de leur énergie cinétique.
Le cas de la centrale nucléaire
La centrale nucléaire est un équipement principalement dévolu à la production d’électricité à partir de la fission nucléaire. Si le principe précédemment énoncé est universel, la mise en œuvre présente des différences que l’on appelle filière. Chaque pays qui en avait les moyens technologiques et financiers a développé sa, voire même ses, propres filières. Pour le principe de fonctionnement, il faut dispose et agencer :
1- une source fissile (un combustible nucléaire) qui saura produire à chaque étape de fission plus d’un neutron;
2- un fluide caloporteur qui saura extraire l’énergie thermique libérée dans les processus de fission. Ce fluide traverse ensuite une turbine où il restitue son énergie thermique qui devient dans la turbine, énergie électrique;
3- un modérateur de neutron. Ceux-ci, dans les processus de fission sont émis avec une énergie cinétique considérable, de sorte que la probabilité de sortie du réacteur est beaucoup plus grande que celle qui entretient la réaction;
4- un système de contrôle constitué d’un absorbeur de neutron qui permet à un opérateur de s’assurer que la réaction en chaîne de fission ne devienne pas divergente.
Il existe plusieurs solutions (filières) dont certaines ont été expérimentées avec succès. Le tableau suivant permet d’en faire les comparaisons.
Tableau 16.3. Comparaison entre les filières de mise en œuvre des centrales nucléaires
| Type de réacteur | Matériau combustible | Matériau modérateur | Fluide caloporteur | Commentaire (filière) |
| UNGG |
U naturel: 0,7 % de 235U |
graphite | CO2 | France :
n’est plus en opération (U naturel-graphite-gaz) |
| CANDU | U naturel | eau lourde | eau lourde sous pression | filière canadienne (U naturel-eau lourde) |
| à eau bouillante | U enrichi à 3 % de 235U | eau naturelle entrant en ébullition dans le cœur du réacteur | filière développée aux États-Unis et en
Suède (U enrichi-eau bouillante) |
|
| à eau sous pression | U enrichi à 3 % de 235U | eau sous pression maintenue à l’état liquide | très classique en occident et en ex-URSS
(appelé VVER) (U enrichi-eau sous pression) |
|
| RMBK | U enrichi à 2-2,6 % de 235U | graphite | eau sous pression | URSS : cas de Tchernobyl! |
| à neutrons (RNR) | U enrichi ou plutonium | aucun | sodium liquide | utilisation particulière : sous-marins
nucléaires (U enrichi-Na liquide) |
Le surgénérateur est une filière développée en particulier par la France. Son principe : il produit plus de combustible nucléaire qu’il en consomme. Cet énoncé quelque peu provocateur mérite quelques explications. C’est un réacteur à neutrons rapides refroidi au sodium liquide. Le cœur est constitué d’une charge d’oxyde d’uranium et d’oxyde de plutonium (le matériau fissile) en proportion de 85-15. La masse de plutonium dans le réacteur atteint 5 tonnes dans le cas du réacteur Superphénix". Autour de ce cœur sont disposées des revêtements chargés initialement en uranium naturel. En cours de fonctionnement, et en 1 année, le réacteur consomme 800 kg de plutonium et libère une énergie électrique de plusieurs Twh. En même temps, l’uranium-238 absorbe une partie des neutrons (voir ci-haut) et le cœur du réacteur produit 640 kg de plutonium et le revêtement 320, soit un total de 960 kg de plutonium. On a donc un bilan net de 160 kg de plutonium. On double ainsi la quantité initiale de plutonium en 31 ans Fig. 16.6)..
|
|
Figure 16.6. Schématisation du fonctionnement du surgénérateur.
On voit donc, que le réacteur, s’il produit plus d’atomes fissiles qu’il en consomme, il le fait au dépens de l’uranium naturel. Cette filière, a priori fort intéressante, suite à de multiples pressions d’ordre politique, stratégique et autre, a été abandonnée. En fait, l’utilisation du sodium liquide constitue la principale préoccupation en matière de sécurité. Les coûts associés à cette utilisation et les dangers potentiels avec une tolérance zéro deviennent élevés et annulent une partie des avantages espérés.
Puisqu’on était parvenu à libérer l’énergie excédentaire contenue dans les noyaux lourds sous forme de "packing fraction" on pouvait peut être aussi libérer celle qui est contenue dans les noyaux légers. On étudia systématiquement les réactions entre noyaux légers et, en particulier celles qui mettaient en jeu les protons ou des deutérons que l’on pouvait aisément accélérer. On trouva que :
| 16.7 |
|
se produit avec une probabilité assez grande, qu’elle dégage une énergie énorme (17,6 Mev) et que cette énergie est communiquée aux neutrons produits qui peuvent la communiquer de proche en proche. En dehors de l’accélérateur de particule, cette réaction pouvait être initiée et maintenue par une température extrêmement élevée qui permettait aux divers noyaux de se rencontrer avec des énergies cinétiques très grandes, d’où son nom de réaction thermonucléaire. Dans la bombe à hydrogène, cette température très élevée nécessaire à l’initiation est fournie par une bombe classique à l’uranium ou au plutonium. Les neutrons produits maintiennent ensuite la température à une valeur suffisante pendant la durée de l’explosion. Les divers perfectionnements de cette technique sont tenus évidemment secrets.
Dans certaines étoiles un cycle thermonucléaire mettant en jeu le carbone a pu être observé (cycle de BETHE) :
1H + 12C 13N 1H + 13C 1H + 14N 15O 1H + 15N |
® 13N + g ® 13C + ß+ + n ® 14N + g ® 15O + g ® 15N + ß+ + n ® 12C + 4He |
__________________________________________________________
TOTAL: 4 1H ® 3 g + 2 b+ + 2 n + 4He + 25 MeV.
|
Il existe plusieurs méthodes de synthèse de nouveaux noyaux toutes basées sur le bombardement d’une cible (un noyau) par un projectile constitué d’un noyau quelconque : le proton, le rayonnement a, le neutron jusqu’à des noyaux relativement lourds. La synthèse de nouveaux noyaux a des applications en médecine nucléaire. L’industrie de l’électronucléaire repose sur la fission de noyaux très gros (transuraniens) alors que la fusion nucléaire utilise l’énergie libérée dans l’interpénétration de noyaux légers. Ce sont les processus de fission qui font fonctionner le soleil et les étoiles.
|
| 8.1 | Compléter les réactions nucléaires suivantes :
|
| 8.2 | Dans le phénomène de diffusion des neutrons cinétiquement excités, en appliquant les principes de conservation habituels, retrouver les formules 16.4 et 16.5. |
| 8.3 | Le radium se désintègre spontanément selon la réaction suivante :
en libérant une énergie de 4,88 MeV. En supposant que l’atome de radium est au repos au moment de la désintégration, en utilisant le principe de la conservation de la quantité de mouvement, calculer l’énergie cinétique de chacun des produits de désintégration. Calculer l’énergie initiale de chacun des atomes créés. |
Réponse : vitesse de l'atome d'hélium = 1,52 107 m/s.
| 8.4 | Quelle est l’énergie dégagée par la réaction de fission nucléaire
On donne :
Combien de moles de carbone faudrait-il brûler pour obtenir la même énergie? C + O2 ® CO2 DH = - 393,5 kJ / mol. |
|
Réponse : 470 tonnes. |
| 8.5 | L’énergie colossale rayonnée continuellement par les étoiles et le Soleil a sa source dans des réactions de fusion nucléaire assez diverses selon la température interne de l’étoile considérée. Dans le cas du Soleil, une étoile relativement froide (environ 10 millions de degrés), on admet que la réaction globale suivante est la source énergétique : 4 1H ® 4He + 2 ß+ + énergie a- La Terre reçoit du Soleil sous forme de rayonnement une énergie estimée à 0,135 J/(cm2·s). En déduire la diminution de masse du Soleil (en tonnes par seconde) sachant que la distance Terre-Soleil est évaluée à 150 000 000 km. b- Quelle est la quantité d’hydrogène consommé par seconde? On admet que la masse d’hydrogène disponible dans le Soleil est de 2 1027 tonnes, calculez la durée de vie possible du Soleil. |
Réponse : 100 milliards d'années.
Exemples de lectures complémentaires
Étiévant, C., L’énergie thermonucléaire, Collection "Que sais-je?", Presses universitaires de France, nº 1017, 1962.
Lewiner, C., Les centrales nucléaires, Collection "Que sais-je?", Presses universitaires de France, nº 1037, 1988.
Divers auteurs, J. Chem. Educ., 76(3), 331-352 (1999).
H. Belhadj-Tahar et M.-H. Darbieu, Application de la chimie de coordination du technétium 99 dans le domaine de la biologie et de la médecine, L’Actualité chimique, 57-63, nov.-déc. 2003.
Dans la revue L'actualité chimique de la Société
chimique de France, deux dossiers intéressants et complémentaires, sur
l'industrie nucléaire en France:
1- "Le cycle du
combustible nucléaire : de la mine d'uranium jusqu'au recyclage et aux déchets",
Paul Rigny, pages I-XIII, N° 345, octobre 2010.
2- " Les
déchets nucléaires et leur gestion", Paul Rigny, Bernard Bonin et Jean-Marie
Gras, pages I-XII, N° 346, novembre 2010.
Relativement à la préparation de divers éléments transuraniens, voir : Chem. & Engin. News, 9 juin 2008, pages 42-43.
Sur le NET :
Histoire nucléaire vue du Canada : http://www.cns-snc.ca/history (visité le 2019-02-19)
Un site web général en français (et bien fait) en provenance du CEA de France :
:http://www.cea.fr/comprendre/Pages/energies/nucleaire/essentiel-sur-reacteurs-nucleaires-du-futur.aspx (visité le 2019-02-19)
Visitez le site du CEA en France.
The ChemWeb News Letter, 16 avril 2010.
Voir aussi : International team
discovers element 117,
Et des PRIX NOBEL :
BETHE :
https://www.nobelprize.org/prizes/physics/1967/bethe/lecture/ (visité
le
2019-02-19).
CHADWICK : https://www.nobelprize.org/prizes/physics/1935/chadwick/biographical/ (visité le 2019-02-19).
O. HAHN :
https://www.nobelprize.org/prizes/chemistry/1944/summary/ (visité
le
2019-02-19).
Dernière mise à jour : 2021-07-23.
________________________________________-