
Sarah-Jane Barnes
Julie Fredette
Unité d'Enseignement en Sciences de la Terre
Université du Québec à Chicoutimi
Février 2001
Sauvegarder ce document sous format *.doc
(1385 Ko)
Retour à la
page principale
Introduction
Les éléments du groupe de platine (EGP) regroupent des
éléments apparentés dont le platine (Pt), le palladium
(Pd), le rhodium (Rh), le ruthénium (Ru), l'iridium (Ir), l'osmium
(Os) et le rhénium (Re). Les EGP sont caractérisés
par des propriétés variées et uniques tel que leur
inertie chimique, leur excellente capacité catalytique, leur point
de fusion élevé, leur résistance à la corrosion
et à l'oxydation sous haute température, leur faible coefficient
d'expansion thermique, leur durabilité mécanique et leurs
propriétés thermoélectriques stables. Étant
donné leurs propriétés, les EGP servent à de
nombreuses applications. Ils sont utilisés soit à l'état
pur ou alliés entre eux ou à d'autres éléments.
Marchés et Prix
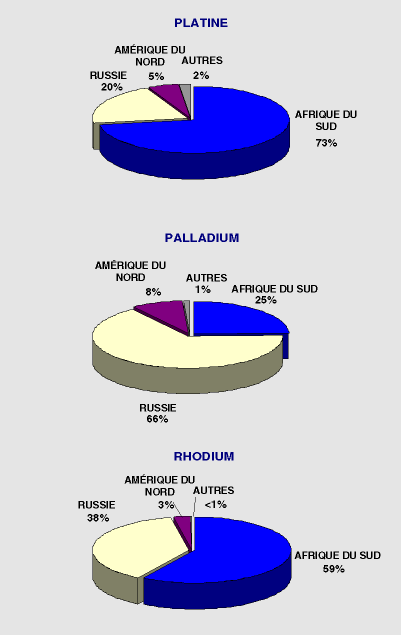
Les principaux pays producteurs de EGP sont l'Afrique du Sud et la Russie
(figure 1). Les États-Unis et le Canada
occupent respectivement le 3e et 4e rang. En 2000,
la production de EGP a été estimée à 5,06 millions
d'onces avec une demande de 5,69 millions onces, une augmentation de 2
% de la demande par rapport à 1999. Le Canada compte un producteur
de EGP comme produit principal et deux producteurs de EGP comme sous-produits.
Depuis quelques années, la demande pour les EGP dans le secteur
industriel des pays à économie de marché excède
l'offre, occasionnant ainsi une augmentation des prix entre 1999 et 2000
(figure 2). La figure 3
présente les prix des EGP (en $/onces) pour les dernières
années.
Consommations et Utilisations
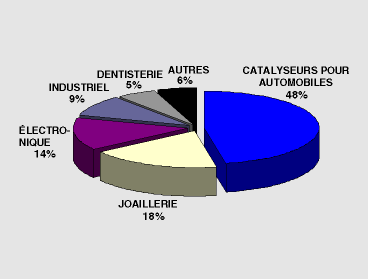
Comme le démontre la figure 4, le secteur
de consommation le plus important de EGP pour les pays à économie
de marché sont les catalyseurs pour automobiles. L'industrie des
EGP étant donc actuellement liée à celle de l'automobile,
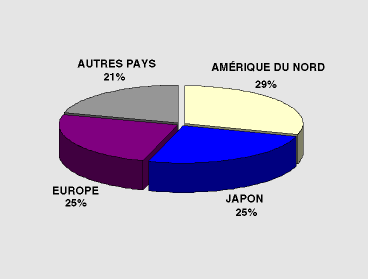
les pays consommateurs de EGP les plus importants sont l'Amérique
du Nord, le Japon, et l'Europe (figure 5).
Le platine et le palladium sont les deux EGP les plus abondamment utilisés.
Avec le rhodium, ils sont surtout utilisés dans les catalyseurs,
en particulier les catalyseurs pour automobiles. Les autres secteurs de
consommation sont l'industrie de l'automobile en général,
l'électronique, la dentisterie, la joaillerie, l'industrie du verre,
les industries chimiques, électriques, le secteur industriel, les
investissements et les piles à combustibles.
Catalyseurs pour automobiles
Les premières lois limitant les émissions par les automobile
ont été adoptées aux États-Unis vers la fin
des années 60. Au Canada, la réglementation sur les émissions
est entrée en vigueur en 1987. Les limites concernant les émissions
ont été progressivement resserrées et des catalyseurs
à oxydation se sont avérés nécessaires pour
permettre de respecter les limites portant sur la pollution de l'air. Dans
les convertisseurs catalytiques pour automobiles, le platine transforme
efficacement les hydrocarbures (HC) et le monoxyde de carbone (CO) des
gaz d'échappement en substances moins nocives, alors que le rhodium
traite plus efficacement les oxydes d'azote (NOx). Le palladium permet
de traiter ces trois polluants, mais de manière moins efficace que
le platine ou le rhodium. Un aspect important est que plus un catalyseur
contient de EGP moins il y a d'émissions polluantes. La composition
des catalyseurs pour automobiles varie selon le prix des différents
EGP, la composition de l'essence, la durée de vie des composantes
et les limites imposées par la réglementation. Le nombre
de pays où les émissions sont réglementées
ne cesse de s'accroître et les réglementations déjà
en place deviennent de plus en plus sévères pour faire face
à l'accroissement de la densité des véhicules automobiles.
Par exemple, en janvier 2000, la phase III de la nouvelle réglementation
quant aux émissions polluantes est entrée en vigueur en Europe.
Dans le secteur de l'essence comme dans celui du diesel, ces nouvelles
réglementations plus strictes ont donc eu un impact direct sur l'industrie
des EGP, contraignant les constructeurs automobiles a utilisés plus
de EGP sur les catalyseurs, contribuant ainsi à l'accroissement
de la demande totale pour les EGP.
Industrie de l'électronique
L'industrie de l'électronique emploie le platine dans certains
substrats pour fabriquer des disques durs d'ordinateur afin d'améliorer
la capacité mémoire des disques. En l'an 2000, 90% des disques
durs contenaient du platine comparativement à 75 % en 1999.
L'emploi de palladium dans le secteur de l'électronique s'est
accru parallèlement à la forte croissance de la demande de
produits électroniques comme les ordinateurs personnels, les téléphones
cellulaires et les caméras vidéo. Les nouvelles générations
d'équipement électronique utilisent davantage de condensateurs
céramiques multicouches (MLCC) contenant du palladium.
De son côté, le ruthénium est utilisé dans
la fabrication de résistors, qui se retrouvent dans presque tous
les appareils électroniques (téléphones cellulaires,
ordinateurs personnels, caméras numériques, etc.). A l'heure
actuelle, l'iridium est utilisé dans la fabrication de creusets
afin de fabriquer des cristaux aux applications électroniques.
Industrie du verre
L'industrie du verre a recourt au platine pour fabriquer des fibres
de verre, tirant avantage de la résistance à la corrosion
et de la résistance mécanique de ce métal. L'une des
applications prometteuses secondaires qui pourraient se traduire par un
accroissement de la consommation future de platine et de rhodium est la
fabrication d'écrans de cristaux liquides (LCD), déjà
utilisés sur les ordinateurs portatifs, et dans des caméras
numériques. De plus, les LCD subissent une utilisation croissante
sur les écrans de télévisons et d'ordinateurs personnels.
Piles à combustible
Une des utilisations les plus intéressantes et prometteuses à
long terme des EGP sont les piles à combustibles. La première
pile à combustible date du 19e siècle, mais les
premières applications "commerciales" des piles à combustible
furent les programmes spatiaux du début des années 60. Le
principe de la pile à combustion est basé sur la conversion
directe de l'énergie chimique d'une réaction en énergie
électrique en utilisant un procédé électrochimique
contrôlé (au lieu d'une réaction thermique de combustion,
dont le travail mécanique engendré est ensuite converti en
électricité). L'énergie est produite en combinant,
sans les mélanger, un combustible (hydrogène, méthanol,
monoxyde de carbone ...) et de l'oxygène (provenant généralement
de l'air) pour produire de l'eau et de l'énergie. Le platine est
utilisé comme enduit catalyseur sur les électrodes des piles.
On peut obtenir l'hydrogène par électrolyse, ce qui nécessite
de l'électricité. Il est aussi possible de l'obtenir après
reformage d'un hydrocarbure comme le méthane ou d'un dérivé
comme le méthanol. Trois éléments sont donc nécessaires
pour la production de piles à combustible: l'eau comme source d'hydrogène,
l'électricité pour produire l'hydrogène et du platine
comme enduit catalyseur.
Une pile à combustible se différencie des autres piles
(ou batteries) électrochimiques par le fait que les réactifs
sont renouvelés et les produits évacués en permanence.
Dans une pile classique, les matériaux constituant les électrodes
sont consommables. Avec le temps, en fonction de l'usage, ils se dégradent
(oxydation de l'anode et réduction de la cathode) pour finalement
rendre le processus inactif, la pile devient usée. Dans une pile
à combustible, la structure (électrodes, électrolyte
et sites réactifs) ne réagit pas, et reste invariante dans
le temps. Un point important est que le rendement électrique des
piles à combustible est supérieur à tous les autres
systèmes connus de générations électriques
(40 à 80% d'efficacité). Les piles à combustible peuvent
être utilisées en mode stationnaire ou mobile (pour la propulsion
de véhicules individuels, de transports collectifs et de transports
de frets). Divers types de piles à combustible sont présentement
à l'étude. Celle offrant le plus de possibilités commerciales
est la pile à combustible à membrane échangeuse de
protons (PEMFC).
Les PEMFC semblent être, à court et moyen termes, les systèmes
les plus prometteurs, car elles sont à la fois compatibles avec
les besoins de la traction automobile et de la cogénération
stationnaire.
Les piles à combustibles existent donc depuis un certain temps
mais la possibilité de les utiliser comme source d'énergie
dans des véhicules est récente et les nombreuses possibilités
qu'offrent cette nouvelle utilisation constitue une augmentation de la
demande en platine. Depuis les années 1970, de nombreux constructeurs
automobiles et entreprises industrielles financent, avec des aides institutionnelles,
de gros efforts de recherche et développement, dans le cadre de
programmes nationaux ou multinationaux de diversification énergétique
ou de protection de l'environnement. En janvier 2001 la compagnie Ballard
a mis sur pied sa première usine de production à Vancouver,
La production potentielle de l'usine est de 30 000 piles par an. Les piles
sont pour le moment destinées aux prototypes développés
par les clients de Ballard (Ford, General Motors, Toyota, Nissan, Baimler
Chrysler et Honda). Selon les plus récentes estimations, la commercialisation
se fera dès 2004 et en 2020, le quart des nouveaux véhicules
automobiles seraient équipées avec une pile à combustible.
De plus, BMW envisage un réseau de distribution d'hydrogène
en Europe pour 2010.
Les piles à combustible sont donc versatiles, efficaces et représentent
une source d'énergie non polluante avec de l'eau comme seul sous-produit.
La diminution inéluctable des ressources fossiles de la planète
et la pression environnementale face aux émissions atmosphériques
encouragent fortement l'utilisation d'énergies propres comme celles
produites par les piles à combustibles. Elles s'inscrivent dans
le cadre de contraintes environnementales de "zéro pollution" et
dans le développement d'une nouvelle génération de
voitures. Elles constituent donc une alternative intéressante aux
systèmes habituels de conversion d'énergie stationnaire et
mobile.
Le Québec est donc bien positionné pour profiter de l'expansion
de l'industrie des piles à combustible car il renferme d'importantes
réserves en eau et d'électricité. La province possède
également du magnésium et de l'aluminium en quantité,
matériaux de base entrant dans la fabrication de voitures légères
fonctionnant avec les piles à combustible. La seule ressource actuellement
absente au Québec pour la fabrication de voitures utilisant des
piles à combustibles sont les EGP, utilisés comme catalyseur.
Autres utilisations
Les EGP sont utilisés dans de nombreux autres secteurs. La joaillerie
représente une industrie toujours très forte pour le platine
ainsi que pour le palladium. L'industrie chimique et le raffinage du pétrole
utilisent du platine et du palladium pour accélérer et améliorer
les réactions chimiques. La dentisterie emploi du palladium dans
les alliages dentaires et les appareils orthodontiques. Et présentement,
on utilise des alliages d'iridium-ruthénium dans les électrodes
des usines de fabrication de chloro-alcali.
Conclusion
A cause de leurs propriétés variées et uniques,
les EGP se substituent difficilement avec d'autres éléments.
Les EGP sont utilisés dans certains secteurs traditionnels mais
l'industrie des EGP est fortement liée à leurs applications
dans de nouvelles technologies. Dans ce contexte économique de nouvelles
technologies, l'étude des EGP permet de quantifier et de bien comprendre
la genèse des gisements existants. En retour, ces études
permettront la découverte de nouveaux gisements. Les deux forces
mondiales en terme de réserves et production de EGP, l'Afrique du
Sud et la Russie, connaissent présentement d'énormes changements
socio-politiques et culturels, ce qui engendre une certaine incertitude
et instabilité dans l'approvisionnement en EGP. Il devient donc
important d'identifier et de définir de nouvelles réserves
de EGP afin de subvenir aux besoins en EGP à court, moyen et long
terme.
Sources générales d'information
Bezian, J.J. 1998. Systèmes de piles à combustible pour
la cogénération: État de l'art.Rapport réalisé
pour le compte de l'ADEME. Centre d'Énergétique de l'École
des Mines de Paris, 44 pages.
Johnson Matthey. 2000. Platinum 2000, Interim Review. Johnson Matthey
Public Limited Company, Londres, Grande-Bretagne, 28 pages.
Johnson Matthey. 1999. Platinum 1999, Interim Review. Johnson Matthey
Public Limited Company, Londres, Grande-Bretagne, 28 pages.
Johnson Matthey. 1998. Platinum 2000, Interim Review. Johnson Matthey
Public Limited Company, Londres, Grande-Bretagne, 28 pages.
McCutcheon, B. 1996. Les métaux du groupe platine. Annuaire des
minéraux du Canada. Ressources naturelles du Canada.
Pearce, F. 2000. Kicking the habit. New Scientist, Vol 168, No 2266,
p.34-42.
Figure 1:
Principaux pays producteurs pour l'année 2000
Haut
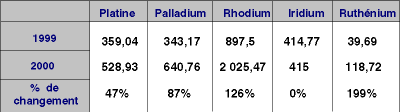
Figure 2:
Prix des EGP en $/onces pour les années 1999 et 2000
Haut
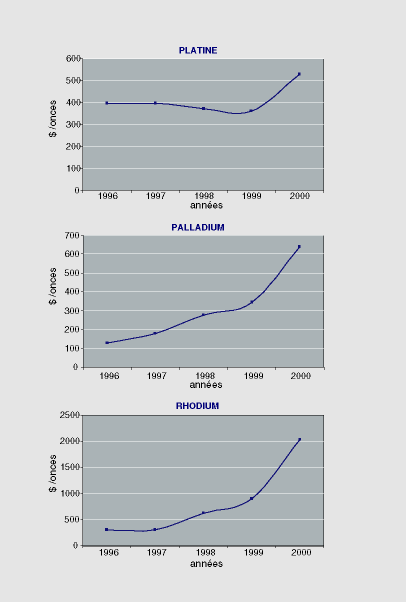
Figure 3:
Prix moyens du Pt, Pd et Rh de 1996 à 2000($/onces)
Haut
Figure 4:
Principaux secteurs de consommation de EGP pour l'année 2000($/onces)
Haut
Figure 5:
Consommation totale de Pt, Pd et Rh par pays pour l'année 2000
Haut
Retour à la
page principale |